Pengertian Dan Struktur Ion
Wednesday, February 12, 2020
Edit
Suatu zat sanggup dibagi-bagi menjadi bagian-bagian (partikel) yang ukuran partikelnya lebih kecil. Partikel terkecil dari suatu zat yang masih memiliki sifat sama dengan sifat asal partikel itu disebut molekul.
Senyawa dari molekul ini sanggup berupa ikatan antara unsur yang sama (molekul unsure), tetapi sanggup juga berupa ikatan antara unsure-unsur yang berbeda (molekul senyawa). Jika suatu senyawa dielektrolisis dengan arus listrik searah maka akan terionisasi. Partikel dari senyawa yang terionisasi ini disebut ion.
A. Pengertian Ion
Atom selain bergabung membentuk molekul sanggup juga membentuk ion. Ion ialah atom atau kelompok atom yang bermuatan listrik. Ion dibedakan menjadi dua, yaitu ion yang bermuatan listrik faktual disebut kation dan ion yang bermuatan listrik negatif disebut anion.
B. Struktur Ion
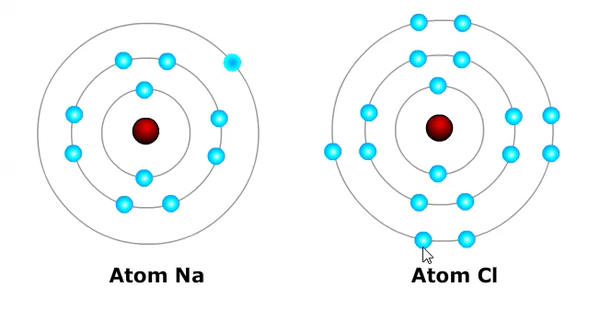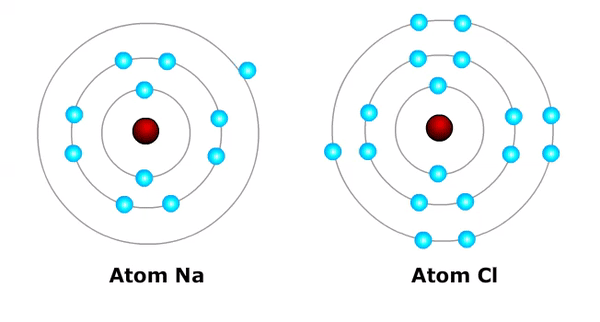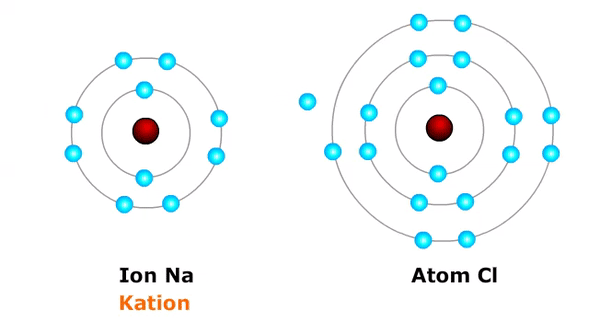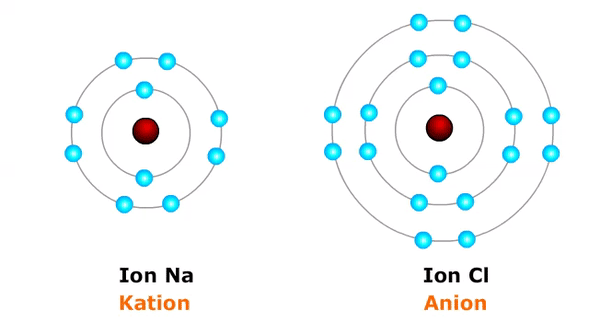
Pada keadaan normal, suatu atom tidak bermuatan atau netral. Ion suatu atom akan terbentuk saat atom melepas atau mendapatkan elektron.
Ion faktual atau kation terbentuk saat sebuah atom kehilangan atau melepaskan elektron, contoh:
Ion negatif atau anion terbentuk saat sebuah atom mendapatkan atau menerima perhiasan elektron, contoh:
Akibatnya, atom yang kehilangan elektron akan menjadi atom yang bermuatan listrik faktual (ion positif/kation) alasannya jumlah proton menjadi lebih besar daripada jumlah elektronnya, sedangkan atom yang kedatangan elektron menjadi atom bermuatan listrik negatif (ion negatif/ anoda) alasannya jumlah elektronnya melebihi jumlah protonnya.
Peristiwa terurainya suatu zat menjadi ion-ion disebut ionisasi. Hasil ionisasi disebut ion. Elektron yang sanggup keluar atau masuk ke suatu atom ialah elektron yang berada di kulit terluar. Ionisasi atom hanya terjadi pada atom-atom yang jumlah elektronnya sama dengan 8, 18, atau 32. Atom-atom yang jumlah elektronnya sama dengan bilangan-bilangan tersebut sangat sukar terionisasi sehingga disebut unsur gas mulia.
Jumlah electron yang terlepas atau masuk tergantung pada jumlah elektron pada kulit terluar dengan ketentuan sebagai berikut:
Beberapa pola kation dan anion sanggup kau lihat pada tabel berikut ini.
C. Senyawa Ion
Suatu senyawa yang terusun dari ion-ion dinamakan senyawa ion. Contoh senyawa ion ialah soda api (natrium hidroksida = NaOH) yang tersusun dari ion faktual natrium (Na+) dan ion negatif hidroksida (OH-).
Contoh lain senyawa ion ialah garam dapur (natrium klorida = NaCl). Jika garam dapur dilarutkan dalam air, maka akan terionisasi menjadi ion faktual natrium (Na⁺)dan ion negatif klorida (Cl⁻).
Contoh penggabungan antara ion-ion faktual dan ion-ion negatif beberapa senyawa ion lainnya diperlihatkan oleh tabel berikut:
Senyawa dari molekul ini sanggup berupa ikatan antara unsur yang sama (molekul unsure), tetapi sanggup juga berupa ikatan antara unsure-unsur yang berbeda (molekul senyawa). Jika suatu senyawa dielektrolisis dengan arus listrik searah maka akan terionisasi. Partikel dari senyawa yang terionisasi ini disebut ion.
A. Pengertian Ion
Atom selain bergabung membentuk molekul sanggup juga membentuk ion. Ion ialah atom atau kelompok atom yang bermuatan listrik. Ion dibedakan menjadi dua, yaitu ion yang bermuatan listrik faktual disebut kation dan ion yang bermuatan listrik negatif disebut anion.
B. Struktur Ion
Pada keadaan normal, suatu atom tidak bermuatan atau netral. Ion suatu atom akan terbentuk saat atom melepas atau mendapatkan elektron.
Ion faktual atau kation terbentuk saat sebuah atom kehilangan atau melepaskan elektron, contoh:
- Na → Na⁺ + e⁻ (atom natrium Na, melepaskan satu elektron menjadi ion natrium bermuatan positip satu = Na+)
- Mg → Mg²⁺ + 2e⁻ (atom magnesium Mg, melepaskan dua elektron menjadi ion magnesium bermuatan dua positip = Mg²⁺)
Ion negatif atau anion terbentuk saat sebuah atom mendapatkan atau menerima perhiasan elektron, contoh:
- Cl + e⁻ → Cl⁻ (atom klorin mendapatkan satu elektron menjadi ion klorin bermuatan negatip satu = Cl⁻)
- O + 2e⁻ → O2⁻ (atom oksigen mendapatkan dua elektron menjadi ion oksigen bermuatan dua negatif = O²⁻).
Akibatnya, atom yang kehilangan elektron akan menjadi atom yang bermuatan listrik faktual (ion positif/kation) alasannya jumlah proton menjadi lebih besar daripada jumlah elektronnya, sedangkan atom yang kedatangan elektron menjadi atom bermuatan listrik negatif (ion negatif/ anoda) alasannya jumlah elektronnya melebihi jumlah protonnya.
Peristiwa terurainya suatu zat menjadi ion-ion disebut ionisasi. Hasil ionisasi disebut ion. Elektron yang sanggup keluar atau masuk ke suatu atom ialah elektron yang berada di kulit terluar. Ionisasi atom hanya terjadi pada atom-atom yang jumlah elektronnya sama dengan 8, 18, atau 32. Atom-atom yang jumlah elektronnya sama dengan bilangan-bilangan tersebut sangat sukar terionisasi sehingga disebut unsur gas mulia.
Jumlah electron yang terlepas atau masuk tergantung pada jumlah elektron pada kulit terluar dengan ketentuan sebagai berikut:
- Jika jumlah electron terluar kurang dari 4 elektron maka atom ini cenderung melepaskan elektron.
- Jika jumlah elektron terluar antara 4 dan 8 maka atom ini cenderung mendapatkan elektron, jumlah electron yang diterima atau dilepaskan menciptakan jumlah electron di kulit itu menjadi 8.
- Jika jumlah elektron pada kulit terluar sama dengan 4 maka atom ini sanggup melepas atau mendapatkan elektron, tergantung dengan unsur apa atom itu berinteraksi.
- Jika jumlah elektron pada kulit terluar sama dengan 8 maka atom itu sangat sukar melepas maupun mendapatkan elektron. Dengan kata lain atom tersebut stabil.
Beberapa pola kation dan anion sanggup kau lihat pada tabel berikut ini.
| Kation | Nama | Anion | Nama |
|---|---|---|---|
| Na+ | Ion natrium | Cl- | Ion klorida |
| Mg2+ | Ion magnesium | O2- | Ion oksida |
| Al3+ | Ion aluminium | S2- | Ion sulfide |
| H+ | Ion hidrogen | I- | Ion iodide |
| K+ | Ion kalium | CO32⁻ | Ion karbonat |
Suatu senyawa yang terusun dari ion-ion dinamakan senyawa ion. Contoh senyawa ion ialah soda api (natrium hidroksida = NaOH) yang tersusun dari ion faktual natrium (Na+) dan ion negatif hidroksida (OH-).
Contoh lain senyawa ion ialah garam dapur (natrium klorida = NaCl). Jika garam dapur dilarutkan dalam air, maka akan terionisasi menjadi ion faktual natrium (Na⁺)dan ion negatif klorida (Cl⁻).
Contoh penggabungan antara ion-ion faktual dan ion-ion negatif beberapa senyawa ion lainnya diperlihatkan oleh tabel berikut:
| Ion Positif→ | SO₄²⁻ | NO₃⁻ |
|---|---|---|
| Ion Negatif ↓ | ||
| Na⁺ (Natrium) | Na₂SO₄ | NaNO₃ |
| Ca²⁺(Kalsium) | CaSO₄ | Ca(NO₃)₂ |
| Al³⁺(Aluminium) | Al₂(SO₄)₃ | Al(NO₃)₃ |